በጠራራ ፀሐይ ውስጥ አንድ ጠርሙስ ውሃ ለጥቂት ሰዓታት ትተው ትንሽ ሲከፍቱ ትንሽ የ “ጩኸት” ድምጽ ሰምተው ያውቃሉ? ይህ የሆነበት ምክንያት የእንፋሎት ግፊት በሚለው መርህ ምክንያት ነው። በኬሚስትሪ ውስጥ ፣ የእንፋሎት ግፊት በውስጡ ያለው የኬሚካል ንጥረ ነገር በሚተንበት ጊዜ (ወደ ጋዝ ሲቀየር) በተዘጋ ኮንቴይነር ግድግዳዎች የሚጫነው ግፊት ነው። በተወሰነ የሙቀት መጠን የእንፋሎት ግፊትን ለማግኘት የ Clausius-Clapeyron ቀመር ይጠቀሙ ln (P1/P2) = (ΔHእንፋሎት/አር) ((1/T2) - (1/T1)).
ደረጃ
ዘዴ 1 ከ 3-የክላውሲየስ-ክላፔየር ቀመርን በመጠቀም
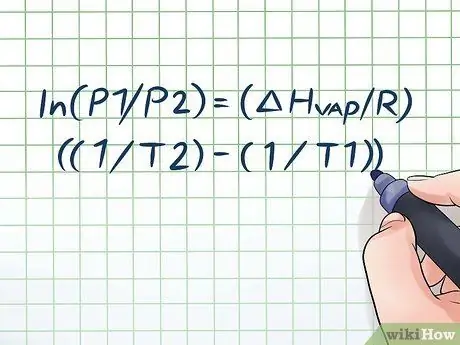
ደረጃ 1. የ Clausius-Clapeyron እኩልታን ይፃፉ።
የእንፋሎት ግፊትን በጊዜ ሂደት ከተለወጠው ጋር ለማስላት ጥቅም ላይ የዋለው ቀመር Clausius – Clapeyron equation (የፊዚክስ ሊቅ ሩዶልፍ ክላውሲየስ እና ቤኖት ፖል ማይል ክላፔሮን ተብሎ ይጠራል።) ይህ በመሠረቱ አብዛኛዎቹን የችግር ዓይነቶች ለመፍታት የሚያስፈልግዎት ቀመር ነው የእንፋሎት ግፊት ጥያቄዎች ብዙውን ጊዜ በፊዚክስ እና በኬሚስትሪ ክፍሎች ውስጥ ይገኛሉ። ቀመር እንደዚህ ነው ln (P1/P2) = (ΔHእንፋሎት/አር) ((1/T2) - (1/T1)). በዚህ ቀመር ፣ ተለዋዋጮች ይወክላሉ-
-
ሸእንፋሎት:
አንድ ፈሳሽ የእንፋሎት ማስወገጃ (ኢንዛይም)። ይህ enthalpy ብዙውን ጊዜ በኬሚስትሪ የመማሪያ መጽሐፍ ጀርባ ባለው ጠረጴዛ ውስጥ ሊገኝ ይችላል።
-
አር ፦
እውነተኛው/ሁለንተናዊ ጋዝ ቋሚ ፣ ወይም 8.314 ጄ/(ኬ × ሞል)።
-
ጥ 1 ፦
የእንፋሎት ግፊት የሚታወቅበት የሙቀት መጠን (ወይም የመጀመሪያ ሙቀት)።
-
T2 ፦
የእንፋሎት ግፊት የማይታወቅበት/ሊገኝ የሚፈልገው (ወይም የመጨረሻው የሙቀት መጠን)።
-
P1 እና P2:
በቅደም ተከተል የሙቀት መጠን T1 እና T2 ላይ የእንፋሎት ግፊት።

ደረጃ 2. የሚያውቋቸውን ተለዋዋጮች ያስገቡ።
የ Clausius-Clapeyron እኩልታ ብዙ የተለያዩ ተለዋዋጮች ስላሉት የተወሳሰበ ይመስላል ፣ ግን ትክክለኛው መረጃ ካለዎት ያን ያህል ከባድ አይደለም። አብዛኛዎቹ መሠረታዊ የእንፋሎት ግፊት ችግሮች ሁለት የሙቀት መጠን እሴቶችን እና አንድ የግፊት እሴትን ወይም ሁለት የግፊት እሴቶችን እና አንድ የሙቀት መጠንን ይዘረዝራሉ - አንዴ ያንን ካወቁ ይህንን ቀመር መፍታት በጣም ቀላል ነው።
- ለምሳሌ ፣ የእንፋሎት ግፊቱ 1 ከባቢ አየር (ኤቲኤም) በ 295 ኪ.ሜ ፈሳሽ የተሞላ ኮንቴይነር እንዳለን ይነገረን። የእኛ ጥያቄ - የእንፋሎት ግፊት በ 393 ኪ. እኛ ሁለት የሙቀት እሴቶች እና አንድ የግፊት እሴት አለን ፣ ስለዚህ የ Clausius-Clapeyron ቀመርን በመጠቀም ሌሎች የግፊት እሴቶችን ማግኘት እንችላለን። የእኛን ተለዋዋጮች በመሰካት እናገኛለን ln (1/P2) = (ΔHእንፋሎት/አር) ((1/393) - (1/295)).
- ለ Clausius-Clapeyron ቀመር ሁል ጊዜ የሙቀት መጠኑን መጠቀም እንዳለብዎ ልብ ይበሉ ኬልቪን. የ P1 እና P2 እሴቶች አንድ እስከሆኑ ድረስ ማንኛውንም የግፊት እሴት መጠቀም ይችላሉ።

ደረጃ 3. ቋሚዎችዎን ያስገቡ።
የ Clausius-Clapeyron እኩልታ ሁለት ቋሚዎች አሉት-አር እና ኤችእንፋሎት. አር ሁል ጊዜ 8.314 ጄ/(ኬ × ሞል) ነው። ሆኖም ፣ ኤችእንፋሎት (የእንፋሎት ማስወጣት) ከላይ እንደተጠቀሰው ፣ አብዛኛውን ጊዜ የ H እሴቶችን ማግኘት ይችላሉእንፋሎት በኬሚስትሪ ወይም በፊዚክስ መማሪያ መጽሐፍ ጀርባ ላሉ የተለያዩ ንጥረ ነገሮች ፣ ወይም በመስመር ላይ (ለምሳሌ ፣ እዚህ)።
-
በእኛ ምሳሌ ውስጥ የእኛ ፈሳሽ ነው እንበል ንጹህ ውሃ።
በሰንጠረ in ውስጥ የ H እሴቶችን ከተመለከትንእንፋሎት፣ ኤችእንፋሎት ንፁህ ውሃ ወደ 40.65 ኪጄ/ሞል ነው። የእኛ ኤች እሴት በጁሎች ውስጥ ስለሆነ ፣ እና ኪሎጁሎች ስላልሆነ ፣ ወደ እሱ መለወጥ እንችላለን 40,650 ጄ/ሞል።
- በእኛ ቋሚዎች ውስጥ መሰካት ፣ እናገኛለን ln (1/P2) = (40,650/8, 314) ((1/393) - (1/295)).
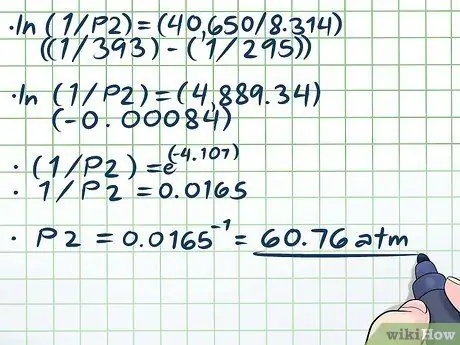
ደረጃ 4. ስሌቱን ይፍቱ።
እርስዎ ከሚፈልጉት በቀር በቀመር ውስጥ ያሉትን ሁሉንም ተለዋዋጮች ካካተቱ በኋላ ፣ በተራ አልጀብራ ደንቦች መሠረት እኩልታውን ወደ መፍታት ይቀጥሉ።
- የእኛን እኩልነት ለመፍታት ብቸኛው አስቸጋሪ ክፍል (ln (1/P2) = (40,650/8, 314) ((1/393) - (1/295))) የተፈጥሮውን ምዝግብ (ln) እየፈታ ነው። የተፈጥሮ ምዝግብ ማስታወሻውን ለማስወገድ ፣ ለሂሳብ ቋሚው ሠ ሠ የሒሳብ ቀጠናውን ሁለቱንም ጎኖች ይጠቀሙ። በሌላ ቃል, ln (x) = 2 → ሠln (x) = ሠ2 → x = ሠ2.
- አሁን የእኛን እኩልነት እንፍታ -
- ln (1/P2) = (40,650/8, 314) ((1/393) - (1/295))
- ln (1/P2) = (4889, 34) (-0, 00084)
- (1/P2) = ሠ(-4, 107)
- 1/P2 = 0.0165
-
P2 = 0.0165-1 = 60 ፣ 76 ኤቲኤም
ይህ ምክንያታዊ ነው - በተዘጋ መያዣ ውስጥ የሙቀት መጠኑን ወደ 100 ዲግሪዎች (ከፈላው ነጥብ ወደ 20 ዲግሪ ያህል ከፍ ማድረግ) ብዙ ግፊትን በፍጥነት ይጨምራል።
ዘዴ 2 ከ 3: በተበታተነ መፍትሄ የእንፋሎት ግፊትን ማግኘት
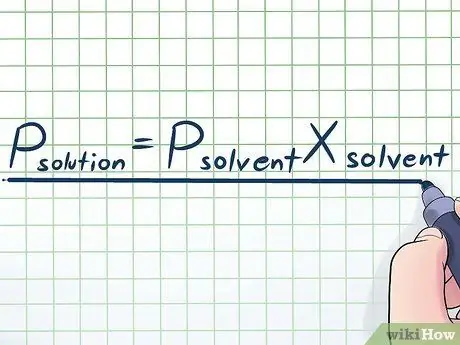
ደረጃ 1. የ Raoult ሕግን ይፃፉ።
በእውነተኛ ህይወት እኛ በንጹህ ፈሳሽ እምብዛም አንሠራም - ብዙውን ጊዜ እኛ ከተለያዩ የተለያዩ ንጥረ ነገሮች ድብልቅ በሆነ ፈሳሽ እንሰራለን። አንዳንድ በብዛት ጥቅም ላይ የሚውሉ ድብልቆች የሚዘጋጁት መፍትሄን ለማዘጋጀት በብዙ ኬሚካሎች ውስጥ ሶሉቴይት የተባለውን የተወሰነ ኬሚካል በትንሽ መጠን በማሟሟት ነው። በእነዚህ አጋጣሚዎች እንደዚህ ተብሎ የተፃፈውን የ Raoult ሕግ (በፊዚክስ ሊቅ ፍራንሷ-ማሪ ራውልት የተሰየመ) ቀመር ማወቅ ጠቃሚ ነው- ገጽsolute= ፒየሚሟሟኤክስየሚሟሟ. በዚህ ቀመር, ተለዋዋጮች ይወክላሉ;
-
ገጽsolute:
የጠቅላላው መፍትሄ የእንፋሎት ግፊት (ሁሉም ንጥረ ነገሮች ተጣምረው)
-
ገጽየሚሟሟ:
የእንፋሎት ግፊት ይቀልጡ
-
ኤክስየሚሟሟ:
የማሟሟት የሞለ ክፍልፋይ
- እንደ ሞለ ክፍልፋይ ያሉ ቃላትን የማያውቁ ከሆነ አይጨነቁ - በሚቀጥሉት ጥቂት ደረጃዎች ውስጥ እናብራራቸዋለን።

ደረጃ 2. በመፍትሔዎ ውስጥ መሟሟቱን ይወስኑ እና ይሟሟሉ።
የተደባለቀ ፈሳሽ የእንፋሎት ግፊት ከመቁጠርዎ በፊት ፣ የሚጠቀሙባቸውን ንጥረ ነገሮች መለየት አለብዎት። ለማስታወስ ያህል ፣ አንድ ፈሳሹ በማሟሟት ውስጥ በሚፈርስበት ጊዜ መፍትሄ ይፈጠራል - የሚሟሟው ኬሚካል ሁል ጊዜ ሶሉቱ ተብሎ ይጠራል ፣ እና እንዲፈርስ የሚያደርገው ኬሚካል ሁል ጊዜ መሟሟት ይባላል።
- የምንወያይበትን ፅንሰ -ሀሳብ ለማሳየት በዚህ ክፍል ውስጥ ያሉትን ቀላል ምሳሌዎች በመጠቀም እንሥራ። ለኛ ምሳሌ ፣ የስኳር ሽሮፕ የእንፋሎት ግፊት ማግኘት እንፈልጋለን እንበል። በተለምዶ ፣ የስኳር ሽሮፕ በውሃ ውስጥ የሚሟሟ ስኳር (1: 1 ጥምርታ) ነው ፣ ስለዚህ እኛ ማለት እንችላለን ስኳር የእኛ መሟሟት እና ውሃ የእኛ መሟሟት ነው።
- ለ sucrose (የጠረጴዛ ስኳር) የኬሚካል ቀመር ሲ መሆኑን ልብ ይበሉ12ሸ22ኦ11. ይህ የኬሚካል ቀመር በጣም አስፈላጊ ይሆናል።
ደረጃ 3. የመፍትሄውን ሙቀት ያግኙ
ከላይ በ Clausius Clapeyron ክፍል ላይ እንዳየነው የአንድ ፈሳሽ የሙቀት መጠን የእንፋሎት ግፊቱን ይነካል። በአጠቃላይ ፣ ከፍ ባለ የሙቀት መጠን ፣ የእንፋሎት ግፊት ይበልጣል - የሙቀት መጠኑ ከፍ እያለ ፣ ብዙ ፈሳሹ ይተን እና እንፋሎት ይፈጥራል ፣ በመያዣው ውስጥ ያለውን ግፊት ይጨምራል።
በእኛ ምሳሌ ውስጥ ፣ በዚህ ጊዜ የስኳር ሽሮፕ የሙቀት መጠኑ ነው እንበል 298 ኪ (ወደ 25 ሴ ገደማ)።
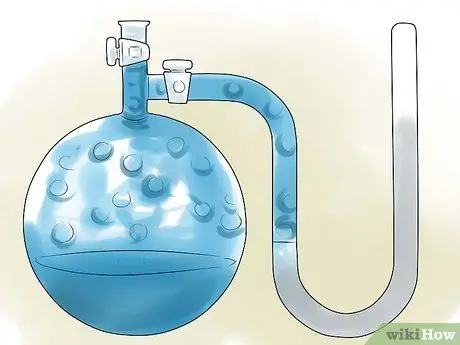
ደረጃ 4. የሟሟውን የእንፋሎት ግፊት ይፈልጉ።
የኬሚካል ማጣቀሻ ቁሳቁሶች ብዙውን ጊዜ ለብዙ የተለመዱ ንጥረ ነገሮች እና ውህዶች የእንፋሎት ግፊት እሴቶች አሏቸው ፣ ነገር ግን እነዚህ የግፊት እሴቶች ብዙውን ጊዜ የሚሠሩት ንጥረ ነገሩ 25 C/298 ኬ የሙቀት መጠን ወይም የመፍላት ነጥብ ካለው ብቻ ነው። መፍትሔዎ ከእነዚህ ሙቀቶች ውስጥ አንዱ ካለው ፣ የማጣቀሻ እሴትን መጠቀም ይችላሉ ፣ ካልሆነ ግን በዚያ የሙቀት መጠን የእንፋሎት ግፊትን ማግኘት ያስፈልግዎታል።
- Clausius -Clapeyron ሊረዳ ይችላል - ለ P1 እና ለ T1 የማጣቀሻ የእንፋሎት ግፊት እና 298 ኪ (25 ሴ) ይጠቀሙ።
- በእኛ ምሳሌ ውስጥ የእኛ ድብልቅ 25 ዲግሪ ሴንቲ ግሬድ አለው ፣ ስለሆነም በቀላሉ የማጣቀሻ ጠረጴዛችንን በቀላሉ መጠቀም እንችላለን። በ 25 C ላይ ውሃ የእንፋሎት ግፊት እንዳለው እናውቃለን 23.8 ሚሜ ኤችጂ

ደረጃ 5. የማሟሟትዎን ሞለኪውል ክፍል ይፈልጉ።
ይህንን ከመፈታታችን በፊት ማድረግ ያለብን የመጨረሻው ነገር የእኛን የማሟሟት ሞለኪውል ክፍል ማግኘት ነው። የሞለኪውል ክፍልፋዩን ማግኘት ቀላል ነው -ውህዶችዎን ወደ ሞሎች ብቻ ይለውጡ ፣ ከዚያ የእያንዳንዱን ውህደት መቶኛ በቁስሉ ውስጥ ባለው የሞሎች ብዛት ውስጥ ያግኙ። በሌላ አነጋገር የእያንዳንዱ ውህድ ሞለኪውል ክፍል እኩል ነው (የተቀላቀሉ አይሎች)/(በቁስ ውስጥ ያሉ የሞሎች ብዛት)።
-
ለስኳር ሽሮፕ አጠቃቀማችን የምግብ አዘገጃጀት እንበል 1 ሊትር (L) ውሃ እና 1 ሊትር ሱክሮስ (ስኳር)።
በዚህ ሁኔታ የእያንዳንዱን ግቢ ሞሎች ብዛት ማግኘት አለብን። ይህንን ለማድረግ የእያንዳንዱን ውህደት ብዛት እናገኛለን ፣ ከዚያ የእቃውን ሞላ ብዛት በመጠቀም ወደ ሞለስ ይለውጡት።
- ብዛት (1 ሊትር ውሃ) - 1,000 ግራም (ሰ)
- ቅዳሴ (1 ሊ ጥሬ ስኳር) - በግምት 1,056 ፣ 8 ግ
- ሞለስ (ውሃ) - 1,000 ግራም × 1 ሞል/18.015 ግ = 55.51 ሞል
- ሞለስ (ሱክሮስ) - 1,056 ፣ 7 ግራም × 1 ሞል/342.2965 ግ = 3.08 ሞሎች (ከኬሚካዊ ቀመርው ፣ ከሱ ኬሚካላዊ ቀመር C ማግኘት እንደሚችሉ ልብ ይበሉ12ሸ22ኦ11.)
- ጠቅላላ አይጦች 55.51 + 3.08 = 58.59 ሞል
- የሞለ የውሃ ክፍል 55 ፣ 51/58 ፣ 59 = 0, 947
ደረጃ 6. ጨርስ።
በመጨረሻም ፣ የእኛን የሬውል ሕግ እኩልታ ለመፍታት የሚያስፈልጉን ነገሮች ሁሉ አሉን። ይህ ክፍል በጣም ቀላል ነው - በዚህ ክፍል መጀመሪያ ላይ በቀለለው የ Raoult ሕግ ቀመር ውስጥ ላሉት ተለዋዋጮች የእርስዎን እሴቶች ያስገቡ። ገጽsolute = ፒየሚሟሟኤክስየሚሟሟ).
- እሴቶቻችንን በማስገባት ፣ እኛ እናገኛለን-
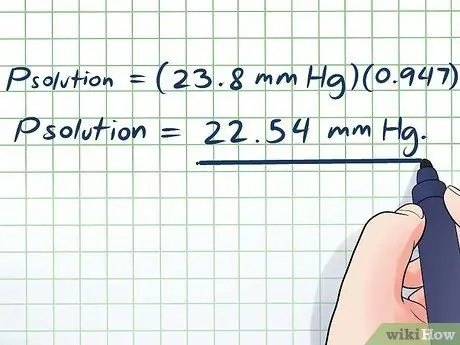
- ገጽመፍትሄ = (23.8 ሚሜ ኤችጂ) (0 ፣ 947)
-
ገጽመፍትሄ = 22.54 ሚሜ ኤችጂ።
ውጤቱ ትርጉም ያለው ነው - በሞለኪዩል አኳያ ፣ በብዙ ውሃ ውስጥ የሚሟሟ በጣም ትንሽ ስኳር አለ (ምንም እንኳን በእውነተኛው ዓለም ፣ ሁለቱም ንጥረ ነገሮች ተመሳሳይ መጠን ቢኖራቸውም) ፣ ስለዚህ የእንፋሎት ግፊት በትንሹ ብቻ ይቀንሳል።
ዘዴ 3 ከ 3 - በልዩ ጉዳዮች ውስጥ የእንፋሎት ግፊት መፈለግ

ደረጃ 1. ከመደበኛ የሙቀት መጠን እና የግፊት ሁኔታዎች ጋር ጥንቃቄ ያድርጉ።
የሳይንስ ሊቃውንት ብዙውን ጊዜ ለአጠቃቀም ቀላል “መደበኛ” የሙቀት እና የግፊት እሴቶችን ስብስብ ይጠቀማሉ። እነዚህ እሴቶች መደበኛ የሙቀት መጠን እና ግፊት (ወይም STP) ይባላሉ። የእንፋሎት ግፊት ችግሮች ብዙውን ጊዜ የ STP ሁኔታዎችን ያመለክታሉ ፣ ስለሆነም እነዚህን እሴቶች ማስታወስ አስፈላጊ ነው። የ STP እሴቶች እንደሚከተለው ይገለፃሉ
- የሙቀት መጠን 273 ፣ 15 ኪ / 0 ሐ / 32 ረ
- ግፊት 760 ሚሜ ኤችጂ / 1 ኤቲኤም / 101 ፣ 325 ኪሎፓስካልስ

ደረጃ 2. ሌሎቹን ተለዋዋጮች ለማግኘት የ Clausius-Clapeyron እኩልታን እንደገና ያዘጋጁ።
በክፍል 1 በምሳሌአችን ፣ ለንፁህ ንጥረ ነገሮች የእንፋሎት ግፊትን ለማግኘት የ Clausius – Clapeyron ቀመር በጣም ጠቃሚ መሆኑን ተመልክተናል። ሆኖም ፣ ሁሉም ጥያቄዎች P1 ወይም P2 ን እንዲፈልጉ አይጠይቁዎትም - ብዙዎች የሙቀት እሴቱን ወይም አንዳንድ ጊዜ የኤች ዋጋን እንዲያገኙ ይጠይቁዎታል።እንፋሎት. እንደ እድል ሆኖ ፣ በእነዚህ አጋጣሚዎች ፣ መልሱን በትክክል ማግኘት በቀላሉ ሊለዩዋቸው የሚፈልጓቸው ተለዋዋጮች በእኩል ምልክቱ በአንድ ወገን ተለያይተው እንዲገኙ ፣ ቀመርን እንደገና የማስተካከል ጉዳይ ብቻ ነው።
- ለምሳሌ ፣ በ 273 ኪ.ግ እና በ 325 ኪ.ሜ በ 150 ቶር የእንፋሎት ግፊት ያልታወቀ ፈሳሽ አለን ፣ እናም የዚህን ፈሳሽ የእንፋሎት (ΔH) የእንፋሎት ማቃጠልን ማግኘት እንፈልጋለን።እንፋሎት). እኛ እንደዚህ ልንፈታው እንችላለን-
- ln (P1/P2) = (ΔHእንፋሎት/አር) ((1/T2) - (1/T1))
- (ln (P1/P2))/((1/T2) - (1/T1)) = (ΔHእንፋሎት/አር)
- R × (ln (P1/P2))/((1/T2) - (1/T1)) = Hእንፋሎት አሁን እሴቶቻችንን እናስገባለን-
- 8, 314 J/(K × ሞል) × (-1, 79)/(-0, 00059) = ሸእንፋሎት
- 8 ፣ 314 ጄ/(ኬ × ሞል) × 3,033 ፣ 90 = ሸእንፋሎት = 25,223 ፣ 83 ጄ/ሞል

ደረጃ 3. ንጥረ ነገሩ እንፋሎት በሚፈጠርበት ጊዜ የሶላቱን የእንፋሎት ግፊት ያሰሉ።
ከላይ ባለው የእኛ የ Raoult Law ምሳሌ ውስጥ የእኛ ሶሉተር ፣ ስኳር ፣ በተለመደው የሙቀት መጠን በራሱ ላይ ምንም ዓይነት ጫና አያደርግም (ያስቡ - ለመጨረሻ ጊዜ የላይኛው ጎድጓዳ ሳህን ውስጥ ስኳር ሲተን ያዩት መቼ ነበር?) ሆኖም ግን ፣ የእርስዎ solute ሲያደርግ ይተናል ፣ ይህ የእንፋሎት ግፊትዎን ይነካል። እኛ የተቀየረውን የ Raoult's Law equation ስሪት በመጠቀም ይህንን እናደርጋለን። ገጽመፍትሄ = (ፒውህደትኤክስውህደት) ምልክቱ ሲግማ (Σ) ማለት የእኛን መልስ ለማግኘት የተለያዩ ውህዶች ሁሉንም የእንፋሎት ግፊቶች መደመር ብቻ ያስፈልገናል ማለት ነው።
- ለምሳሌ ፣ ከሁለት ኬሚካሎች የተሠራ ቤንዚን እና ቶሉኔን መፍትሄ አለን እንበል። የመፍትሄው አጠቃላይ መጠን 12 ሚሊ ሊትር (ሚሊ) ነው። 60 ሚሊ ቤንዚን እና 60 ሚሊ ቶሉሊን። የመፍትሄው የሙቀት መጠን 25 ዲግሪ ሴንቲግሬድ ሲሆን የእያንዳንዳቸው ኬሚካሎች በ 25 ዲግሪ ሴንቲግሬድ ውስጥ የእንፋሎት ግፊቶች ለቤንዚን 95.1 ሚሜ ኤችጂ እና ቶሉዌን 28.4 ሚሜ ኤችጂ ናቸው። በእነዚህ እሴቶች የመፍትሄውን የእንፋሎት ግፊት ያግኙ። ለሁለታችን ኬሚካሎች መደበኛ መጠጋጋት ፣ የሞላ ብዛት እና የእንፋሎት ግፊት እሴቶችን በመጠቀም ይህንን እንደሚከተለው ማድረግ እንችላለን-
- ቅዳሴ (ቤንዚን) 60 ሚሊ = 0.060 ሊ እና ጊዜ 876.50 ኪግ/1,000 ሊ = 0.053 ኪግ = 53 ግ
- ቅዳሴ (ቶሉኔ) - 0.060 ሊ እና ጊዜ 866 ፣ 90 ኪ.ግ/1,000 ሊ = 0.052 ኪግ = 52 ግ
- ሞል (ቤንዚን) - 53 ግ × 1 ሞል/78 ፣ 11 ግ = 0.679 ሞል
- ሞለስ (ቶሉኔ) - 52 ግ × 1 ሞል/92 ፣ 14 ግ = 0.564 ሞል
- ጠቅላላ አይጦች 0.679 + 0.564 = 1.243
- የሞለ ክፍልፋይ (ቤንዚን) - 0.679/1 ፣ 243 = 0.546
- የሞለ ክፍልፋይ (ቶሉኔ) - 0.564/1 ፣ 243 = 0.454
- መፍትሄ - ፒመፍትሄ = ፒቤንዚንኤክስቤንዚን + ገጽቶሉኔንኤክስቶሉኔን
- ገጽመፍትሄ = (95.1 ሚሜ ኤችጂ) (0 ፣ 546) + (28.4 ሚሜ ኤችጂ) (0 ፣ 454)
- ገጽመፍትሄ = 51.92 ሚሜ ኤችጂ + 12.89 ሚሜ ኤችጂ = 64 ፣ 81 ሚሜ ኤችጂ
ጠቃሚ ምክሮች
- ከላይ ያለውን የ Clausius Clapeyron ቀመር ለመጠቀም ፣ የሙቀት መጠኑ በኬልቪን (እንደ ኬ የተፃፈ) መሆን አለበት። በሴልሲየስ ውስጥ የሙቀት መጠን ካለዎት ከዚያ የሚከተለውን ቀመር በመጠቀም መለወጥ አለብዎት። ቲኬ = 273 + ቲሐ
- ከላይ የተጠቀሱት ዘዴዎች ጥቅም ላይ ሊውሉ ይችላሉ ምክንያቱም ጉልበቱ ከተተገበረው የሙቀት መጠን ጋር በትክክል ተመጣጣኝ ነው። የፈሳሹ ሙቀት የእንፋሎት ግፊትን የሚጎዳ ብቸኛው የአካባቢ ሁኔታ ነው።







