ወቅታዊው ጠረጴዛ ግራ የሚያጋባ እና ለመረዳት የሚያስቸግር ሆኖ ካገኙት ፣ አይጨነቁ ፣ ብቻዎን አይደሉም! ወቅታዊው ሠንጠረዥ እንዴት እንደሚሠራ መረዳት ከባድ ሊሆን ይችላል ፣ ግን እንዴት ማንበብ እንደሚችሉ በመማር በሳይንስ ውስጥ ስኬታማ ይሆናሉ። በየወቅታዊው ጠረጴዛ ላይ ያለውን አወቃቀር እና ስለ ንጥረ ነገሮች የሚያሳየውን መረጃ በመረዳት ይጀምሩ። በመቀጠል እያንዳንዱን ንጥረ ነገሮች ማጥናት ይችላሉ። በመጨረሻም ፣ በአቶም ውስጥ ያለውን የኒውትሮን ብዛት ለማወቅ በየወቅታዊው ሰንጠረዥ ላይ የተዘረዘሩትን መረጃዎች ይጠቀሙ።
ደረጃ
የ 3 ክፍል 1 - የወቅታዊውን ሰንጠረዥ አወቃቀር መረዳት
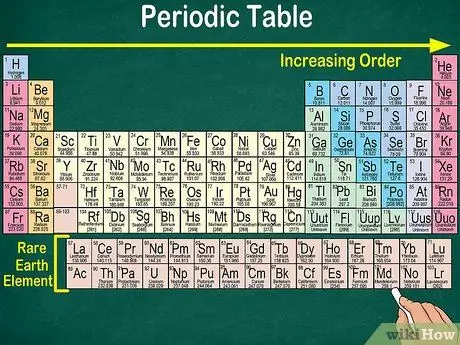
ደረጃ 1. ወቅታዊውን ሰንጠረዥ ከላይ ከግራ ወደ ታች በቀኝ ያንብቡ።
ንጥረ ነገሮቹ በአቶሚክ ቁጥራቸው መሠረት ይደረደራሉ። ወደ ቀኝ እና ወደ ታች ፣ የአቶሚክ ቁጥር ከፍ ይላል። የአቶሚክ ቁጥር የአንድ ንጥረ ነገር አቶም ያለው የፕሮቶኖች ብዛት ነው። ወደ ቀኝ ሲሄዱ ፣ የእያንዳንዱ አቶም የጅምላ ቁጥር እንደሚጨምርም ያስተውላሉ። ማለትም ፣ በጠረጴዛው ላይ ያለውን ቦታ በመመልከት ብቻ የአንድን ንጥረ ነገር ክብደት መረዳት ይችላሉ።
- ወደ ቀኝ ወይም ወደ ታች ፣ የአንድ ንጥረ ነገር አቶሚክ ብዛት ይጨምራል ፣ ምክንያቱም የአቶሚክ ብዛቱ በእያንዳንዱ ኤለመንት ውስጥ ፕሮቶኖችን እና ኒውትሮን በመደመር ይሰላል። የፕሮቶኖች ብዛት ከኤለመንት ጋር ይጨምራል ፣ ይህ ማለት ክብደቱ እንዲሁ ይጨምራል።
- ኤሌክትሮኖች በአቶሚክ ብዛት ውስጥ አይካተቱም ምክንያቱም ከፕሮቶኖች እና ከኒውትሮን ጋር ሲነፃፀሩ ኤሌክትሮኖች በአቶሚክ ክብደት ላይ ብዙም ተጽዕኖ አይኖራቸውም።

ደረጃ 2. እያንዳንዱ ንጥረ ነገር ከግራው አቶም ይልቅ 1 ተጨማሪ ፕሮቶን እንደሚይዝ ይረዱ።
የአቶሚክ ቁጥሩን በመመልከት ይህንን ማወቅ ይችላሉ። የአቶሚክ ቁጥሮች ከግራ ወደ ቀኝ ይደረደራሉ። ንጥረ ነገሮቹ እንዲሁ በ 3 ቡድኖች ተለያይተዋል ፣ በሠንጠረ in ውስጥ መመደቡን ማየት ይችላሉ።
ለምሳሌ ፣ የመጀመሪያው ረድፍ የአቶሚክ ቁጥር 1 ያለውን ሃይድሮጂን ይዘረዝራል ፣ እና አቶሚክ ቁጥር 2. ያለውን ሂሊየም ይዘዋል። ሆኖም ፣ እነዚህ ሁለት አካላት በተለያዩ ቡድኖች ውስጥ ስለሆኑ በጠረጴዛው ግራ እና ቀኝ ይገኛሉ።
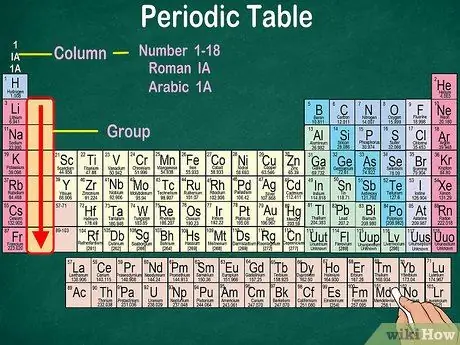
ደረጃ 3. ተመሳሳይ የአካላዊ እና የኬሚካል ባህሪዎች አተሞች ቡድኖችን መለየት።
ቡድኖች በአቀባዊ ዓምዶች ይጠቁማሉ። በአብዛኛዎቹ ሁኔታዎች ቡድኖች በተመሳሳይ ቀለም ተለይተው ይታወቃሉ። ይህ የትኞቹ ንጥረ ነገሮች ተመሳሳይ አካላዊ እና ኬሚካዊ ባህሪዎች እንዳሉ ለመለየት ይረዳዎታል። ይህ የእነዚህን ንጥረ ነገሮች ምላሾች ለመተንበይ ቀላል ያደርግልዎታል። በአንድ ቡድን ውስጥ ያለው እያንዳንዱ ንጥረ ነገር በውጫዊው ምህዋሩ ውስጥ ተመሳሳይ የኤሌክትሮኖች ብዛት አለው።
- አብዛኛዎቹ ንጥረ ነገሮች የአንድ ቡድን ብቻ ናቸው። ሆኖም ሃይድሮጂን እንደ ሃሎጅን ወይም አልካላይ ብረት ተብሎ ሊመደብ ይችላል። በአንዳንድ ጠረጴዛዎች ውስጥ ሃይድሮጂን በሁለቱም ቡድኖች ውስጥ ይታያል።
- በአብዛኛዎቹ አጋጣሚዎች ፣ ዓምዶቹ በሠንጠረ top አናት ወይም ታችኛው ክፍል ላይ 1-18 ይቆጠራሉ። ቁጥሮቹ በሮማን ቁጥሮች (አይአይ) ፣ በአረብ ቁጥሮች (1 ሀ) ወይም በቁጥር (1) ሊታዩ ይችላሉ።
- የአቶሚክ ቡድኖችን ከላይ እስከ ታች ያንብቡ።
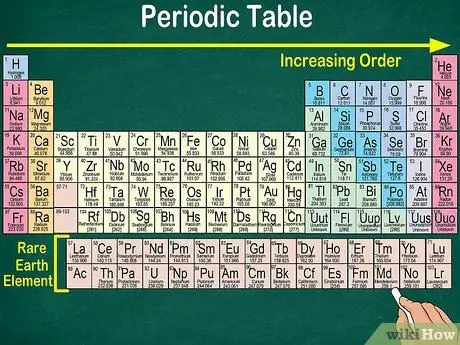
ደረጃ 4. በሠንጠረ in ውስጥ ያለውን ባዶ ቦታ ያስተውሉ።
ከአቶሚክ ቁጥር በተጨማሪ የንጥረ ነገሮች በቡድን እና በቡድን መደራጀት ተመሳሳይ የአካል እና ኬሚካዊ ባህሪያትን ግምት ውስጥ ያስገባል። በዚህ መንገድ ፣ እያንዳንዱ ንጥረ ነገር እንዴት ምላሽ እንደሚሰጥ በተሻለ ይረዱዎታል። የኬሚካል ንጥረ ነገሮች መጨመር ምደባቸውን የበለጠ አስቸጋሪ ያደርገዋል ፣ ስለሆነም ወቅታዊው ጠረጴዛ ባዶ ቦታ መያዙ አያስገርምም።
- ለምሳሌ ፣ የመጀመሪያዎቹ 3 ረድፎች ባዶ ቦታዎች አሏቸው ፣ ምክንያቱም በሰንጠረ in ውስጥ የሚታዩት የሽግግር ብረቶች አቶሚክ ቁጥር 21 ያላቸው አካላት ናቸው።
- በተመሳሳይ ፣ ከ 57 እስከ 71 ያሉት ፣ ያልተለመዱ የምድር አካላት ወይም ያልተለመዱ የምድር ንጥረ ነገሮች ፣ በሠንጠረ bottom ታችኛው ክፍል በስተቀኝ ተለይተው ተገልፀዋል።
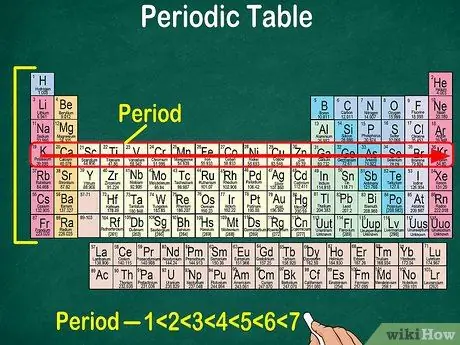
ደረጃ 5. እያንዳንዱ ረድፍ የወር አበባ ተብሎ መጠራቱን ልብ ይበሉ።
በአንድ ጊዜ ውስጥ ያሉት ሁሉም ንጥረ ነገሮች ኤሌክትሮኖች የሚያልፉበት ተመሳሳይ የአቶሚክ ምህዋር አላቸው። የምሕዋር ቁጥር ብዛት ከወቅቶች ብዛት ጋር ይዛመዳል። ወቅታዊ ሰንጠረዥ 7 ረድፎችን ያሳያል ፣ ይህ ማለት 7 ወቅቶች አሉ ማለት ነው።
- ለምሳሌ ፣ በ 1 ጊዜ ውስጥ አንድ አካል 1 ምህዋር አለው ፣ በ 7 ውስጥ ያለው ንጥረ ነገር 7 ምህዋር አለው።
- በአብዛኛዎቹ አጋጣሚዎች ወቅቶቹ ከጠረጴዛው በግራ በኩል ከላይ እስከ ታች ከ1-7 ይቆጠራሉ።
- ረድፉን ከግራ ወደ ቀኝ የተከተሉትን ንጥረ ነገሮች ጊዜ ያንብቡ።
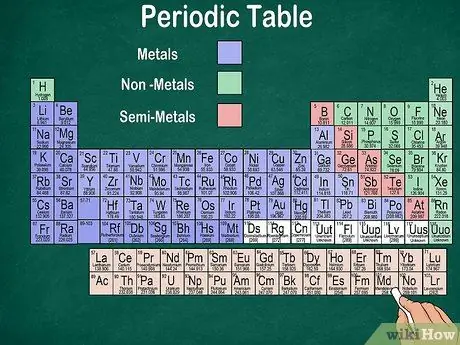
ደረጃ 6. ብረቶችን ፣ ሴሚሜተሎችን እና ባልሆኑ ብረቶችን መለየት።
የኤለመንቱን ዓይነት በመለየት የንጥረቶችን ባህሪዎች በተሻለ መረዳት ይችላሉ። እንደ እድል ሆኖ ፣ አብዛኛው ወቅታዊ ሠንጠረዥ አንድ ንጥረ ነገር ብረት ፣ ሴሚሜታል ወይም ኢ -ሜታል አለመሆኑን ለማመልከት ቀለሙን ይጠቀማል። ከሠንጠረ right በስተቀኝ በኩል የብረት ንጥረ ነገሮችን ያገኛሉ ፣ በግራ በኩል ደግሞ ብረቶች ያልሆኑ። ከፊል-ብረት ቡድኑ በብረት እና ባልሆኑ ብረቶች መካከል ይገኛል።
- በባህሪያቱ ምክንያት ሃይድሮጂን ከ halogens ወይም ከአልካላይን ብረቶች ጋር ሊመደብ እንደሚችል ያስታውሱ። ስለዚህ ፣ ሃይድሮጂን በጠረጴዛው በሁለቱም በኩል ብቅ ማለት ወይም የተለየ ቀለም መሆን ተፈጥሯዊ ነው።
- አንድ ንጥረ ነገር የሚያብረቀርቅ ፣ በክፍሉ የሙቀት መጠን ጠንካራ ፣ ሙቀትን እና ኤሌክትሪክን የሚያከናውን እና ለስላሳ እና ሊለጠጥ የሚችል ከሆነ ብረት ይባላል።
- አንድ ንጥረ ነገር የሚያብረቀርቅ ካልሆነ ፣ ሙቀትን ወይም ኤሌክትሪክን የማያከናውን እና ከባድ ከሆነ እንደ ብረት ያልሆነ ይቆጠራል። እነዚህ ንጥረ ነገሮች አብዛኛውን ጊዜ በክፍል ሙቀት ውስጥ ጋዝ ናቸው ፣ ግን በተወሰኑ የሙቀት መጠኖችም ጠንካራ ወይም ፈሳሽ ሊሆኑ ይችላሉ።
- አንድ ንጥረ ነገር የብረታ ብረት እና የብረታ ብረት ያልሆኑ ጥምር ባህሪዎች ካለው ሴሚሜታል ተብሎ ይጠራል።
ክፍል 2 ከ 3 - ንጥረ ነገሮችን ማጥናት
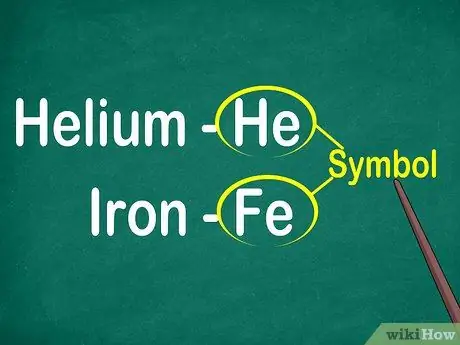
ደረጃ 1. ከ 1 እስከ 2 ፊደል አባላትን ምልክቶች መለየት።
ምልክቱ ብዙውን ጊዜ በትልቁ ቅርጸ -ቁምፊ ባለው ካሬ መሃል ላይ ይገኛል። ምልክቶች በተለያዩ ቋንቋዎች ደረጃቸውን የጠበቁ የአባል ስሞች ምህፃረ ቃላት ናቸው። ሙከራዎችን ሲያካሂዱ ወይም በአንደኛ ደረጃ እኩልታዎች ላይ ሲሠሩ ፣ ምናልባት የአባል ምልክቶችን ይጠቀማሉ። ስለዚህ ፣ ወደድንም ጠላንም እራስዎን ከዋናው ምልክቶች ጋር በደንብ ማወቅ አለብዎት።
ምልክቶች ብዙውን ጊዜ ከላቲን ስም ከኤለመንት ስም የተገኙ ናቸው ፣ ግን አንዳንድ ጊዜ በሰፊው ጥቅም ላይ ከዋሉ ስሞች በተለይም አዲስ አካላት ይወጣሉ። ለምሳሌ ፣ የሄሊየም ምልክት እሱ ነው ፣ እሱም ለዚህ የታወቀ ስም ይቆማል። ሆኖም ፣ የብረት ምልክት ፌ ነው ፣ ይህም በአንደኛው እይታ ላይ በአንፃራዊነት አስቸጋሪ ነው።

ደረጃ 2. የአሉቱን ሙሉ ስም ያግኙ ፣ ካለ።
ሙሉ በሙሉ መፃፍ ካለብዎት የሚጠቀሙበት ንጥረ ነገር ስም ነው። ለምሳሌ ፣ “ሂሊየም” እና “ካርቦን” የንጥረ ነገሮች ስሞች ናቸው። በአብዛኛዎቹ ሁኔታዎች የአባል ስም ከምልክቱ በታች ነው ፣ ግን ምደባው ሊለያይ ይችላል።
አንዳንድ ወቅታዊ ሰንጠረ theች ሙሉውን ስም ላያካትቱ እና ምልክቶችን ብቻ መጠቀም ይችላሉ።
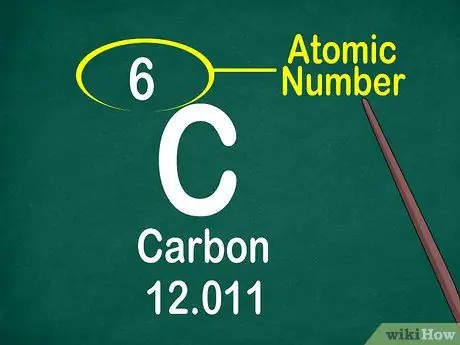
ደረጃ 3. የአቶሚክ ቁጥሩን ልብ ይበሉ።
የአቶሚክ ቁጥሩ ብዙውን ጊዜ በመካከለኛው ወይም በሳጥኑ ጥግ ላይ በሳጥኑ አናት ላይ ይገኛል። ሆኖም ፣ የአቶሚክ ቁጥር እንዲሁ በአባል ምልክት ወይም በአባል ስም ስር ሊገኝ ይችላል። የአቶሚክ ቁጥሮች ከ1-118 የታዘዙ ናቸው።
የአቶሚክ ቁጥሩ ኢንቲጀር እንጂ አስርዮሽ አይደለም።
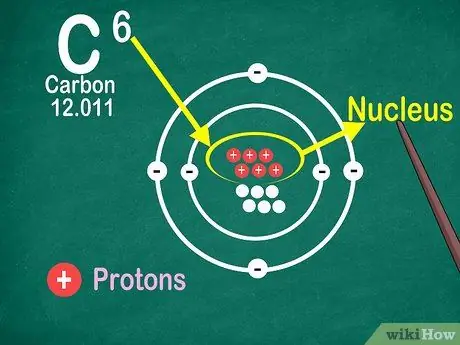
ደረጃ 4. የአቶሚክ ቁጥር በአቶም ውስጥ የፕሮቶኖች ብዛት መሆኑን ይወቁ።
በአንድ ኤለመንት ውስጥ ያሉ ሁሉም አቶሞች ተመሳሳይ የፕሮቶኖች ብዛት አላቸው። እንደ ኤሌክትሮኖች በተቃራኒ ፕሮቶኖች በአቶሞች ሊያዙ ወይም ሊለቀቁ አይችሉም። አቶሞች አተሞችን መያዝ ወይም ማጣት ከቻሉ ንጥረ ነገሮች ይለወጣሉ።
እንዲሁም የኤሌክትሮኖችን እና የኒውትሮን ብዛት ለማወቅ የአቶሚክ ቁጥር ያስፈልግዎታል።
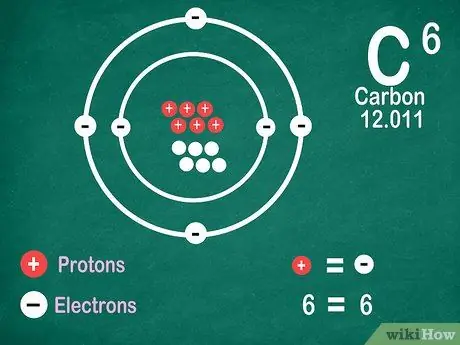
ደረጃ 5. ኤለመንቱ ionization እስካልተደረገ ድረስ ኤለመንቶች ልክ እንደ ፕሮቶኖች ተመሳሳይ የኤሌክትሮኖች ብዛት እንዳላቸው ይወቁ።
ፕሮቶኖች አዎንታዊ ክፍያ አላቸው ፣ ኤሌክትሮኖች አሉታዊ ክፍያ አላቸው። ገለልተኛ አቶም የኤሌክትሪክ ክፍያ ስለሌለው ተመሳሳይ የኤሌክትሮኖች እና ፕሮቶኖች ብዛት አለው ማለት ነው። ሆኖም ፣ አቶሞች ኤሌክትሮኖችን ሊያጡ እና ሊያገኙ ይችላሉ ፣ ይህም ionized ያደርጋቸዋል።
- አዮኖች የኤሌክትሪክ ክፍያዎች ናቸው። በአንድ ion ውስጥ ብዙ ፕሮቶኖች ካሉ ፣ ክፍያው አዎንታዊ ነው ፣ ይህም ከ ion ምልክት ቀጥሎ አዎንታዊ (+) ምልክት ነው። በ ion ውስጥ የኤሌክትሮኖች ብዛት የበለጠ ከሆነ ክፍያው አሉታዊ ነው ፣ እሱም አሉታዊ (-)።
- አቶም ion ካልሆነ አዎንታዊ ወይም አሉታዊ ምልክት አያዩም።
ክፍል 3 ከ 3 - ኒውትሮን ለመቁጠር የአቶሚክ ክብደትን መጠቀም

ደረጃ 1. የአቶሚክ ክብደትን ይወቁ።
የአቶሚክ ክብደት ብዙውን ጊዜ በሳጥኑ ግርጌ ፣ ከኤለመንት ምልክት በታች ይገኛል። አቶሚክ ክብደት ፕሮቶኖችን እና ኒውትሮን ጨምሮ በአቶሚክ ኒውክሊየስ ውስጥ ያሉት ቅንጣቶች ጥምር ክብደት ነው። ሆኖም ion ዎች የመቁጠር ሂደቱን ሊያወሳስቡ ይችላሉ። ስለዚህ የአቶሚክ ክብደት የአማካዩን የአቶሚክ ብዛት እና የአዮኖቹን የአቶሚክ መጠን ያሳያል።
- በአማካይ ክብደታቸው ምክንያት አብዛኛዎቹ አተሞች በአስርዮሽ ቅርፅ የአቶሚክ ክብደት አላቸው።
- የአንድ ንጥረ ነገር ክብደት ከግራ ወደ ቀኝ የሚጨምር ቢመስልም ፣ ያ ሁልጊዜ አይደለም።
ደረጃ 2. የምታጠ areውን ኤለመንት የጅምላ ቁጥር ይወስኑ።
የአቶሚክ ብዛትን በማዞር የጅምላ ቁጥሩን ማግኘት ይችላሉ። ይህ እውነታ የአቶሚክ ክብደት ion ን ጨምሮ የሁሉም የአቶሚክ ብዛት አማካይ መሆኑን ያረጋግጣል።
ለምሳሌ ፣ የካርቦን የአቶሚክ ክብደት 12,011 ስለሆነ እስከ 12 ድረስ ተሰብስቧል።
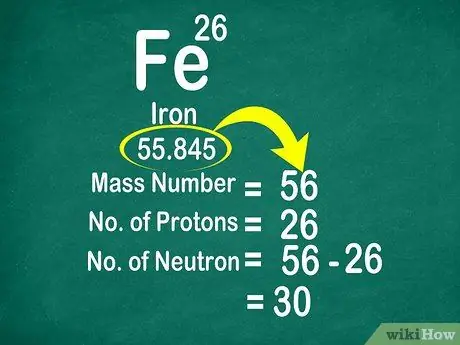
ደረጃ 3. ኒውትሮኖችን ለመቁጠር የጅምላ ቁጥሩን ከአቶሚክ ቁጥር ይቀንሱ።
የጅምላ ቁጥሩ ፕሮቶኖችን ቁጥር ወደ ኒውትሮን ቁጥር በመጨመር ሊሰላ ይችላል። የጅምላ ቁጥሩን ከፕሮቶኖች ብዛት በመቀነስ ይህ በአቶም ውስጥ የኒውትሮን ቁጥርን ማስላት ቀላል ያደርግልዎታል።
- ይህንን ቀመር ይጠቀሙ - ኒውትሮን = የጅምላ ቁጥር - ፕሮቶን
- ለምሳሌ ፣ የካርቦን ብዛት 12 ሲሆን 6 ፕሮቶኖች አሉት። ስለዚህ ካርቦን 6 ኒውትሮን እንዳለው ማወቅ እንችላለን ምክንያቱም 12 - 6 = 6።
- ሌላ ምሳሌ ፣ የብረት ብዛት 56 ሲሆን 26 ፕሮቶኖች አሉት። ስለዚህ ብረት 30 ኒውትሮን እንዳለው እናውቃለን ምክንያቱም 56 - 26 = 30።
- የአቶሞች ኢሶቶፖች የተለያዩ የኒውትሮን ቁጥሮች ይዘዋል ስለዚህ የአቶሚክ ክብደታቸው ይለወጣል።
ጠቃሚ ምክሮች
- ወቅታዊ ሠንጠረዥን ማንበብ ለአንዳንድ ሰዎች ከባድ ነው። ወቅታዊ ሰንጠረዥን ለማጥናት ከከበደህ ተስፋ አትቁረጥ!
- በሠንጠረ in ውስጥ ያሉት ቀለሞች ሊለያዩ ይችላሉ ፣ ግን ይዘቱ እንደቀጠለ ነው።
- አንዳንድ ወቅታዊ ሰንጠረ incomች ያልተሟላ መረጃ ሊሰጡ ይችላሉ። ለምሳሌ ፣ አንዳንድ ሰንጠረ theች ምልክቱን እና የአቶሚክ ቁጥሩን ብቻ ይሰጣሉ። ለዚያ ፣ ለፍላጎቶችዎ የሚስማማ ጠረጴዛ ይፈልጉ!







